以前、呼吸によって肺の中の酸素分圧がどう変化するのかを説明しましたが、今回はその酸素分圧によって血液に中に酸素がどのくらい溶け込むかを求めていきます。
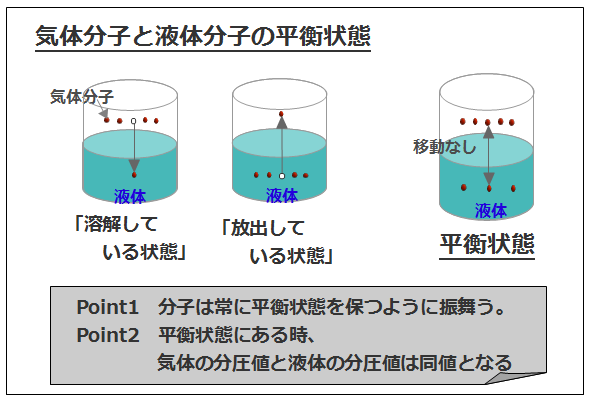
気体と液体の狭間での出来事~平衡状態~
下図のように気体が液体と接したとき、気体の分子は分子構造を崩さずにそのままの状態で液体の中に溶け込むという性質があります。気体の中の分子の数と液体の中の分子数のバランスによって、分子は気体から液体へ、または液体から気体へ移動します。その分子の移動がなくなった時の状態を「平衡状態」といい、分子は常にこの安定した平衡状態を保つように振る舞います。この平衡状態の時、気体の分圧値と液体の分圧値は同じ値として取り扱われます。
液体に溶け込む分子の量~ヘンリーの法則~
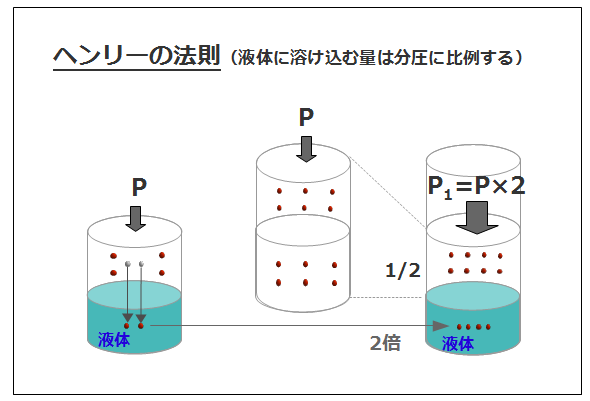
ヘンリーの法則とは、「気体から液体へ溶け込む分子の数は気体の分圧に比例する」というもので、下図を使って具体的に説明します。
Pという一定の圧力によって液体に溶け込んだ分子数が、圧力が2倍になると液体に溶け込む分子数も2倍になることを示しています。酸素カプセルは、酸素分圧を高めて、このヘンリーの法則を利用して血液中に溶け込む酸素量を増やす装置ということになります。
液体への溶け込みやすさ~ブンゼン係数~
気体の分子は、その種類によって水への溶けやすさが違います。例えば、体温と同じ37℃の水なら以下の通りになり、これをブンゼン係数といいます。
|
酸素 |
0.024 |
|---|---|
|
窒素 |
0.012 |
|
二酸化炭素 |
0.570 |
この値は760mmHgの圧力の下での数字なので、酸素の場合21%とした場合1リットルの水に溶け込む酸素量を求めると、
(760×0.21)/760 × 1000[ml] × 0.024 = 5.04[ml]
となります。
血液に溶け込む酸素量の算出
上記のブンゼン係数を用いて1日に血液中に溶け込む酸素量を算出してみます。今回の算出に当たって以下の条件を加えます。
- 心拍数と拍出量は標準的な70回/分と70ml/回とする
- 肺の中の体温は37℃で酸素分圧(=動脈血の酸素分圧)は100mmHgとする
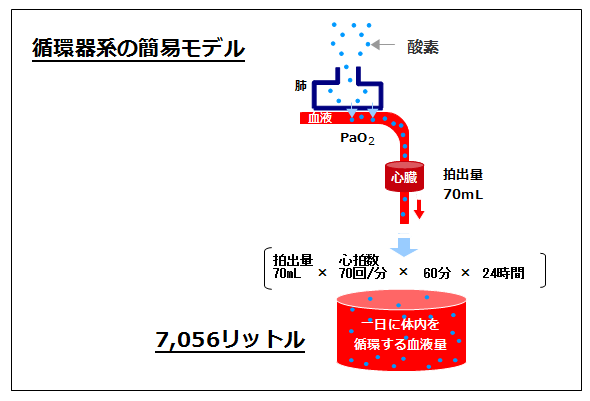
心拍数と拍出量から1日に体内を駆け巡る血液の総量は下記の通り求めることができます。
70ml × 70回/分 × 60分 × 24時間 = 7056リットル
よって1日に血液に溶け込む酸素量は、肺の中の酸素分圧が100mmHgの場合、
100mmHg/760mmHg × 7056リットル × 0.024 = 22リットル
となります。
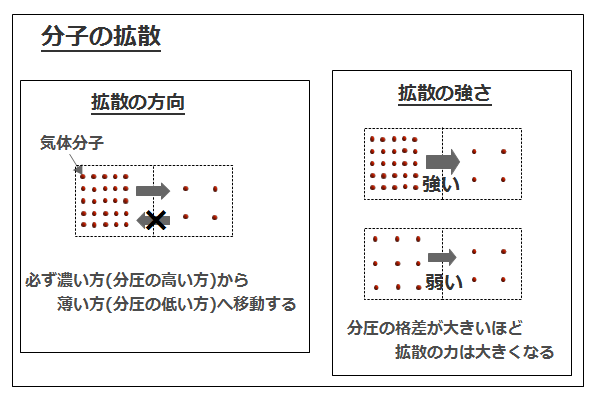
分子の移動~拡散~
酸素分子は体液の中でも煙と同じで”濃い側”から”薄い側”へ拡がっていきます。決して”薄い側”から濃い側”へ集まり益々濃くなることはありません。
これを分圧を使って表現すると、「液体の中の分子は、分圧の高い側から低い側へ移動する」と言い換えることができます。これが拡散です。
また移動する力は、分圧の格差が大きい程拡散する力は強くなりより広範囲に広がっていきます。「酸素カプセルに入ると身体の隅々まで酸素が行き渡る」と言われるのはこの分圧の格差を使って説明することが出来ます。